eISSN 2444-7986
DOI: https://doi.org/10.14201/orl.26047
ARTÍCULO DE REVISIÓN
PRÁCTICA OTORRINOLARINGOLÓGICA DURANTE LA PANDEMIA COVID19
ENT practice during the COVID19 pandemic
Juan Manuel MAZA-SOLANO1; Juan Carlos AMOR-DORADO2; Pablo Luis PARENTE-ARIAS3; Christian Ezequiel CALVO-HENRÍQUEZ4; Guillermo PLAZA-MAYOR5.
1 SAS. Hospital Unversitario Virgen Macarena. Servicio de Otorrinolaringología. Sevilla. España. QUIRONSALUD. Hospital Sagrado Corazón. Servicio de Otorrinolaringología. Sevilla. España. Universidad de Sevilla. Departamento de Cirugía. Sevilla. España.
2 IB-SALUT. Hospital Can Misses. Servicio de Otorrinolaringología. Ibiza. España.
3 SERGAS. Complexo Hospitalario Universitario de A Coruña. Servicio de Otorrinolaringología. A Coruña. España. Hospital HM Rosaleda. Servicio de Otorrinolaringología. Santiago de Compostela. España.
4 SERGAS. Hospital Universitario de Santiago de Compostela. Servicio de Otorrinolaringología. Santiago de Compostela. España.
5 SERMAS. Hospital Universitario de Fuenlabrada. Jefe de Servicio de Otorrinolaringología. Madrid. España. Hospital Sanitas La Zarzuela. Jefe de Servicio de Otorrinolaringología. Madrid. España. Universidad Rey Juan Carlos. Madrid. España.
Correspondencia: juanm.maza.sspa@juntadeandalucia.es
Fecha de recepción: 16 de marzo de 2021
Fecha de aceptación: 18 de marzo de 2021
Fecha de publicación: 20 de marzo de 2021
Fecha de publicación del fascículo: 1 de junio de 2021
Conflicto de intereses: Los autores declaran no tener conflictos de intereses
Imágenes: Los autores declaran haber obtenido las imágenes con el permiso de los pacientes
Política de derechos y autoarchivo: se permite el autoarchivo de la versión post-print (SHERPA/RoMEO)
Licencia CC BY-NC-ND. Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional
Universidad de Salamanca. Su comercialización está sujeta al permiso del editor
RESUMEN
Introducción: La enfermedad por el SARS CoV-2 (COVID-19) ha provocado millones de casos desde que se declarase el estado de pandemia por la Organización Mundial de la Salud (OMS) en marzo de 2020, cambiando las prácticas médicas y quirúrgicas habituales. Los sanitarios representan un importante porcentaje de la población general contagiada. Entre ellos, destaca el especial riesgo de infección en otorrinolaringólogos y cirujanos de cabeza y cuello (ORL), debido a la cercanía a la vía aérea superior y al riesgo de generación de bioaerosoles durante los procedimientos. Objetivo: El objetivo de este artículo es la elaboración de un documento de práctica otorrinolaringológica segura durante la pandemia COVID19. Método: Revisión bibliográfica. Resultados: Recopilación de la mejor evidencia adaptada al riesgo de transmisión, según la combinación de los resultados de los indicadores de riesgo establecidos por el Ministerio de Sanidad, Consumo y Bienestar Social (MSCBS). El presente documento es fruto de la colaboración de las comisiones científicas y del comité COVID-19 de la SEORLCCC.
PALABRAS CLAVE
COVID-19; SARS-Cov-2; COVID-19 Testing; Otolaryngology
SUMMARY
Introduction: The SARS CoV-2 (COVID-19) disease has caused millions of cases since the pandemic status was declared by the World Health Organization (WHO) in March 2020, changing the usual medical and surgical practices. Doctors and nurses represent a significant percentage of the general population infected. Among them, the special risk of infection in otorhinolaryngologists and head and neck surgeons (ENT) stands out, due to the proximity to the upper airway and the risk of generation of bioaerosols during procedures. Objective: The objective of this article is to prepare a document on safe otorhinolaryngological practice during the COVID19 pandemic. Results: Compilation of the best evidence adapted to the risk of transmission, according to the combination of the results of the risk indicators established by the Ministry of Health, Consumption and Social Welfare (MSCBS). This document is the result of the collaboration of the scientific commissions and the COVID-19 committee of the SEORLCCC.
KEYWORDS
COVID-19; SARS-Cov-2; COVID-19 Testing; Otolaryngology
INTRODUCCIÓN
La enfermedad por el SARS CoV-2 (COVID-19) ha provocado más de 100 millones de casos y más de 2 millones de muertes a nivel mundial desde que se declarase el estado de pandemia por la Organización Mundial de la Salud (OMS) en marzo de 2020 [1]. El virus SARS-CoV-2 es un ARN-virus monocatenario de la familia Coronaviridae, estrechamente relacionado con los virus responsables del síndrome respiratorio agudo severo (SARS) y del síndrome respiratorio del Medio Oriente (MERS). Se sospecha que su origen esté asociado con los murciélagos o los manís [2]. La principal vía de entrada del virus es la mucosa de las cavidades oral y nasal. La transmisión se produce mediante el contacto directo desde las manos o los fómites contaminados, o mediante transmisión aérea [3,4]. El periodo de incubación varía entre 2 y 14 días (5,7 días de media) [5], tras lo cual el paciente puede estar asintomático [6] o iniciar una clínica muy variable, cuyas manifestaciones más frecuentes incluyen fiebre, tos seca, disnea, mialgias, fatiga, dolor de cabeza, diarrea, malestar general, anosmia, hiposmia y disgeusia. La enfermedad suele tener una evolución benigna, aunque puede progresar a neumonía bilateral, distrés respiratorio y fallecimiento. Se estima que la tasa de letalidad de la enfermedad es del 0,68% [7], aunque depende en gran medida de la edad y factores de riesgo concurrentes [8]. Una de las mayores dificultades para el control de la enfermedad es la posibilidad de transmisión del agente etiológico por pacientes asintomáticos y presintomáticos [9].
Los sanitarios representan un importante porcentaje de la población general contagiada [10]. Entre los facultativos destaca el especial riesgo de infección en otorrinolaringólogos y cirujanos de cabeza y cuello, debido a la cercanía a la vía aérea superior y al riesgo de generación de bioaerosoles en los procedimientos que realizan (orofaringoscopia, nasofibrolaringoscopia, etc.) [11,12]. La tasa de contagio de especialistas en otorrinolaringología y cirugía de cabeza y cuello (ORL) en España ascendió a 16,5% durante las dos primeras olas [13].
El objetivo de este artículo es la elaboración de un documento de práctica otorrinolaringológica segura durante la pandemia COVID19, basado en una recopilación de la mejor evidencia adaptada al riesgo de transmisión, según la combinación de los resultados de los indicadores de riesgo establecidos por el Ministerio de Sanidad, Consumo y Bienestar Social (MSCBS) [14,15].
DIAGNÓSTICO Y CRIBADO DE PACIENTES COVID-19
DIAGNÓSTICO
1. Presencia del virus
a. Detección de RNA viral. Mediante transcriptasa inversa y reacción en cadena de polimerasa (RT-PCR) se determina la presencia de genes específicos del virus SARS-CoV-2 en muestras de la vía aérea, por lo que indica presencia del virus aunque no capacidad para transmitirlo. La RT-qPCR proporciona una estimación cuantitativa mediante una señal de fluorescencia que aumenta proporcionalmente a la cantidad de ácido nucleico amplificado. La prueba informa de la cantidad de virus presente en la muestra mediante la detección de un umbral especificado en un cierto número de ciclos (Ct o umbral de ciclo) en la RT-PCR [16,17].
b. Presencia de antígenos del virus (antígenos S, M y E) en las secreciones de la vía aérea. Presentan un elevado número de falsos negativos en función de la fase de la enfermedad en que se estudian. Actualmente, el test rápido de detección del antígeno viral se considera de elección en pacientes sintomáticos en el ámbito ambulatorio o en grandes cribados de población. Presenta una elevada sensibilidad en pacientes con síntomas de menos de 5 días de evolución, aunque ante una prueba negativa, si la sospecha clínico-epidemiológica es alta, se debe realizar RT-PCR [18].
2. Estudio de los anticuerpos en sangre-suero. En pacientes con formas graves de COVID-19 se ha descrito la detección de anticuerpos IgM a partir del 7º día desde el inicio de los síntomas, considerándose un signo de la respuesta inmune del paciente (18). A partir de los 14 días se inicia la producción de anticuerpos IgG, cuyo interés reside en su posible efecto de respuesta duradera. Los casos en los que se detecta IgM e IgG elevadas, podrían suponer situaciones intermedias de infección e inmunización. La determinación de anticuerpos podría considerarse útil ante un paciente altamente sospechoso de tener COVID-19 con RT-PCR negativa. Además, hasta un 20% de los pacientes con formas leves de la COVID-19 no presentan anticuerpos en suero [17,19]. El estudio de anticuerpos se puede realizar mediante:
a. Pruebas rápidas de detección de presencia de anticuerpos: Se basan en la inmunocromatografía (técnica de flujo lateral) y se han popularizado como «pruebas rápidas» de detección de anticuerpos [20]. Se recomienda su uso para estudios epidemiológicos en grupos de riesgo [21].
b. Pruebas de laboratorio para medición del nivel de anticuerpos: emplean la técnica de ensayo por inmunoabsorción ligado a enzimas (ELISA) o de quimioluminiscencia (CLIA). Son pruebas cuantitativas y tienen mayor sensibilidad y especificidad. Están estandarizadas y se interpretan fácilmente, pero precisan personal especializado para su realización [21].
INTERPRETACIÓN DE LAS PRUEBAS DIAGNÓSTICAS
La determinación de la presencia del virus debe realizarse mediante RT-PCR ya que su precisión diagnóstica es superior a las pruebas que detectan la presencia de los antígenos de la cápside viral. La presencia de anticuerpos en los pacientes COVID-19 debe interpretarse siempre teniendo en cuenta el resultado de la RT-PCR y la fase clínica de la enfermedad. Una RT-PCR positiva debe considerarse como paciente potencialmente infeccioso. La presencia de anticuerpos IgM e IgG deben orientarnos sobre la respuesta del huésped frente al virus, que podrían relacionarse con inmunidad específica, pero no podemos considerar el estado infeccioso o contagioso del paciente si no disponemos de la RT-PCR [22].
Se necesitan resultados de estudios de seroprevalencia en sujetos de la población general que no hayan sufrido la enfermedad, o hayan padecido formas leves, que informen del verdadero significado de la presencia de anticuerpos en suero, que expliquen si la respuesta inmune es realmente protectora, así como cuánto dura dicha protección [17].
TRANSMISIBILIDAD Y FINALIZACIÓN DEL AISLAMIENTO
La duración de la transmisibilidad varía entre pacientes asintomáticos, leves y graves. En general se ha establecido, que no existe posibilidad de transmisión del virus a partir del noveno día del final de los síntomas [23], aunque en pacientes graves o severos, este punto puede ser difícil de establecer.
En la población general no se considera necesaria la realización de RT-PCR para finalizar el confinamiento, dado que ésta sólo nos informará de la existencia de RNA viral, no de su transmisibilidad [24]. En los pacientes asintomáticos aislados en su domicilio, se pondrá fin al confinamiento a los 10 días de la realización de la prueba. En pacientes sintomáticos, la duración del confinamiento será de 10 días desde la resolución de la fiebre y el cuadro clínico. En los pacientes graves, el periodo de aislamiento domiciliario podrá ser de 21 días. En el caso de personal sanitario se recomienda realizar al menos una prueba diagnóstica para su reincorporación al finalizar el periodo de aislamiento, ya sea determinación de IgG o RT-PCR [15].
CRIBADO GENERAL DEL PACIENTE ORL CANDIDATO A CIRUGÍA O DE UNA EXPLORACIÓN INVASIVA DE LA VÍA AÉREA SUPERIOR
Durante la pandemia es recomendable realizar un cribado de infección activa por SARS-CoV-2 a todos los pacientes que vayan a acudir a una consulta, realizar una exploración invasiva o ser sometidos a una cirugía. La elección de las pruebas variará en función del escenario de alerta según la escala de actuaciones de respuesta coordinada para el control de la transmisión de la COVID-19 publicada por el MSCBS del Gobierno de España en 2020 [25, 26, 27].
El cribado clínico-epidemiológico debe ser realizado por el personal sanitario o socio-sanitario a todos los pacientes pendientes de cirugía, con la antelación suficiente y si es posible de forma no presencial. El cribado microbiológico e inmunológico se realizará mediante RT-PCR, y debe realizarse lo más cercana posible al procedimiento a realizar por el otorrinolaringólogo (72 horas previas), y que el paciente mantenga una situación de aislamiento domiciliario hasta entonces. El cribado no estará basado en el test de antígenos [12].
En función del escenario de alerta específico en cada territorio y dependiendo de los criterios epidemiológicos se recomienda para el cribado de la infección activa lo siguiente:
1. En los escenarios de nivel de alerta 2 o superiores (epidemiología desfavorable), se debe realizar el despistaje completo prequirúrgico, (Tabla 1) (Figura 1).
2. Si la epidemiología del área o territorio sanitario es favorable (nivel de alerta 1), y con riesgo del paciente o cirugía intermedios, se podría omitir la RT-PCR (Tabla 1) (Figura 2):
3. Si la epidemiología del área es favorable, en nivel de alerta 1 y con riesgo del paciente intermedio y cirugía de riesgo bajo, se podrá simplificar el despistaje (Tabla 1) (Figura 2).
Tabla 1. Indicadores para la valoración del riesgo por COVID-19 [14].
INDICADORES |
FÓRMULA DE CÁLCULO |
VALORACIÓN DEL RIESGO |
|||||
NUEVA NORMALIDAD |
BAJO |
MEDIO |
ALTO |
MUY ALTO |
|||
BLOQUE I: Evaluación del nivel de transmisión. |
|||||||
T1 |
Incidencia acumulada de casos diagnosticados en 14 días. |
Casos confirmados (por fecha de diagnóstico) en 14 días *100.000 / nº de habitantes. |
≤25 |
>25 a ≤50 |
>50 a ≤150 |
>150 a ≤250 |
>250 |
T1’ |
Incidencia acumulada de casos diagnosticados en 7 días. |
Casos confirmados (por fecha de diagnóstico) en 7 días *100.000 / nº de habitantes. |
≤10 |
>10 a ≤25 |
>25 a ≤75 |
>75 a ≤125 |
>125 |
T2 |
Incidencia acumulada de casos con ≥65 años diagnosticados en 14 días. |
Casos ≥65 años confirmados (por fecha de diagnóstico) en 14 días *100.000 / nº de habitantes ≥ 65 años. |
≤20 |
>20 a ≤50 |
>50 a ≤100 |
>100 a ≤150 |
>150 |
T2’ |
Incidencia acumulada de casos con ≤65 años diagnosticados en 7 días. |
Casos ≤65 años confirmados (por fecha de diagnóstico) en 7 días *100.000 / nº de habitantes ≤65 años. |
≤10 |
>10 a ≤25 |
>25 a ≤50 |
>50 a ≤75 |
>75 |
T3 |
Positividad global de las pruebas diagnósticas de infección activa (PDIA) por semana. |
Nº de pruebas con resultado positivo en 7 días *100 / Nº de pruebas realizadas en 7 días. |
≤4% |
>4% a ≤7% |
>7% a ≤10% |
>10% a ≤15% |
>15% |
T4 |
Porcentaje de casos con trazabilidad. |
Nº de casos diagnosticados con trazabilidad *100 / Nº total de casos confirmados diagnosticados los últimos 7 días. |
>80% |
≤80% a >65% |
≤65% a >50 |
≤50% a >30% |
≤30% |
BLOQUE II: nivel de utilización de servicios asistenciales por COVID-19 |
|||||||
A1 |
Ocupación de camas de hospitalización por casos de COVID-19 |
Nº de camas de hospitalización ocupadas por casos de COVID / Nº total de camas de hospitalización en funcionamiento. |
≤2% |
>2% a ≤5% |
>5% a ≤10% |
>10% a ≤15% |
>15% |
A2 |
Ocupación de camas de cuidados críticos por casos de COVID-19 |
Nº de camas de cuidados críticos ocupadas por casos de COVID / Nº total de camas de cuidados críticos totales en funcionamiento. |
≤5% |
>5% a ≤10% |
>10% a ≤15% |
>15% a ≤25% |
>25% |
Niveles de alerta: nivel de alerta 1: Cuando al menos dos indicadores del Bloque I y uno del Bloque II están en nivel bajo; nivel de alerta 2: Cuando al menos dos indicadores del Bloque I y uno del Bloque II están en nivel medio; nivel de alerta 3: Cuando al menos dos indicadores del Bloque I y uno del Bloque II están en nivel alto; nivel de alerta 4: Cuando al menos dos indicadores del Bloque I y uno del Bloque II están en nivel muy alto.
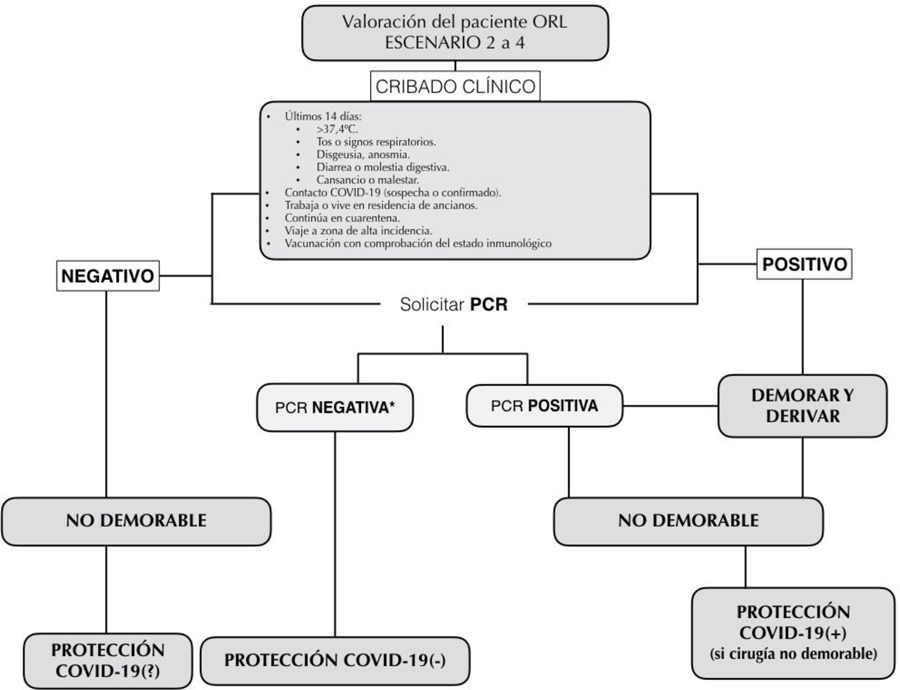
Figura 1. Cribado del paciente otorrinolaringológico en Niveles de Alerta 2 o superior de la pandemia COVID-19.
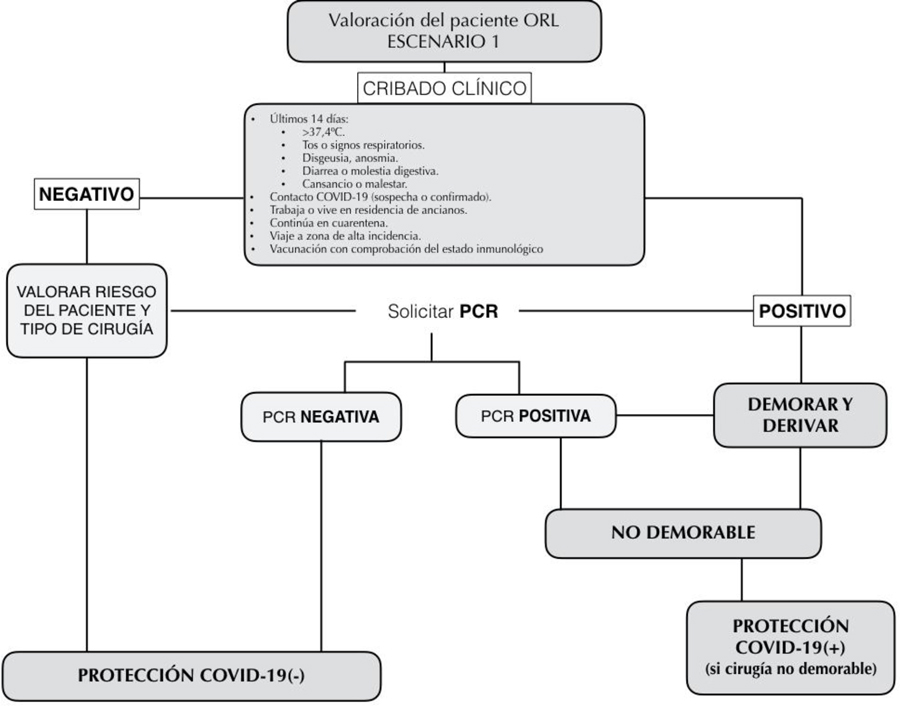
Figura 2. Cribado del paciente otorrinolaringológico en nivel de alerta 1 o inferior de la pandemia COVID-19.
En los casos en los que se haya suspendido la cirugía se seguirán las recomendaciones de retirada del aislamiento recogido en la estrategia basada en pruebas de laboratorio del Documento de Prevención y Control de la infección en el manejo de pacientes con COVID-19 [12], y se realizará una nueva valoración clínica para la actualización de la preanestesia y de posibles secuelas tras la COVID-19 antes de una nueva programación electiva del procedimiento. Los pacientes ingresados en los que se les programe una cirugía electiva seguirán el proceso de despistaje de manera similar a los pacientes ambulatorios, necesitando la repetición de la prueba diagnóstica, si estuviese indicada, en las 72 horas previas a la cirugía, independientemente de que la tuviera realizada con anterioridad.
Actualmente se consideran pacientes con infección pasada a los asintomáticos con serología IgG positiva, así como a los que han tenido un episodio activo con RT-PCR (+) hace más de 10 días (21 en pacientes críticos) y que están asintomáticos desde al menos 3 días.
En pacientes con infección resuelta documentada en los últimos 6 meses, en ausencia de síntomas o datos de alarma en el cuestionario clínico epidemiológico, no será necesario realizar la RT-PCR. Pero en función de la situación clínica, se retrasará la cirugía hasta 4 semanas desde el inicio de los síntomas [15].
Actualmente, no existe evidencia sobre la situación de infectividad y transmisibilidad de pacientes vacunados. Por este motivo, y hasta tener más información, se recomienda que sean considerados como no inmunizados.
MEDIDAS DE PROTECCIÓN NO QUIRÚRGICAS PARA OTORRINOLARINGÓLOGOS Y CIRUJANOS DE CABEZA Y CUELLO
Durante la pandemia por la COVID-19, el uso de equipos de protección individual (EPI) debe ser obligatorio, incluyendo los periodos de tiempo en los que se evidencien indicios de mejoría del estado de la pandemia, y hasta que se reintroduzca la normalidad asistencial. Junto a las precauciones básicas que incluyen el uso de ropa de trabajo y mascarillas quirúrgicas desechables, se han definido tres grados de precauciones contra la transmisión aérea. Las precauciones de grado I incluyen el uso de ropa de trabajo específica (pijamas desechables), gorro médico impermeable, mascarilla quirúrgica, bata y guantes de látex. Las de grado II incluyen el uso de un gorro médico impermeable, máscara N95/FFP2, bata de aislamiento anti-penetración, guantes de látex, cubiertas para zapatos y el uso de gafas protectoras antivaho o una careta protectora si existe el riesgo de producción de gotas virales [28]. Y las precauciones de grado III incluyen todo el equipo de protección personal de grado II, así como mascarillas de tipo FFP3 y respiradores purificadores de aire motorizados [29] (Tabla 2).
Tabla 2. Precauciones individuales en función de la gradación del riesgo de contagio [29].
|
GRADO 1 |
GRADO 2 |
GRADO 3 |
ROPA DE TRABAJO |
Pijama desechable |
Pijama desechable |
Pijama desechable |
PROTECCIÓN DE LA CABEZA |
Gorro médico impermeable |
Gorro médico impermeable |
Gorro médico impermeable |
MASCARILLA |
Quirúrgica |
N95/FFP2 |
FFP3 |
BATA |
Simple Sin aislamiento |
Bata de aislamiento Antipenetración |
Bata de aislamiento Antipenetración |
GUANTES |
Látex. |
Látex |
Látex |
CALZADO |
No cubierto. |
Cubierto |
Cubierto |
PROTECCIÓN OCULAR |
- |
Gafas Pantallas |
Gafas Pantallas |
RESPIRADORES PURIFICADORES DE AIRE MOTORIZADO |
- |
- |
+ |
En pacientes hipoacúsicos el uso de mascarillas especialmente diseñadas para la labiolectura puede utilizarse siempre y cuando no exista un riesgo potencial para el profesional, o si se está realizando un procedimiento con riesgo de aerosolización. En este supuesto, se le explicará el procedimiento con la mascarilla de labiolectura y una pantalla facial al paciente, y posteriormente el sanitario se colocará el tipo de mascarilla que proceda [30,31]. El lavado de manos y la desinfección con geles hidroalcohólicos, se seguirá llevando a cabo en base a las recomendaciones de la OMS [32,33].
Se recomienda una adecuada accesibilidad a la información, ya sea de manera física (carteles, folletos, etc.) en lugares estratégicos o vía online (webs y apps), donde se indiquen los requerimientos obligatorios como el uso de mascarilla, la distancia de seguridad o la higiene de manos [34], además de infografía sobre el mantenimiento de un tono de voz silencioso para evitar la superdiseminación del virus que sucede por la gran cantidad de aerosoles emitidos cuando se emplea un tono de voz elevado [35]. Estos espacios deben estar adaptados con dispensadores con solución hidroalcohólica, contenedores de residuos con tapa de apertura con pedal y asientos adecuadamente separados e indicados que ayuden a mantener la distancia de seguridad entre las personas.
La telemedicina se ha implementado durante la pandemia en muchos servicios, y si se dispone de ella, debería utilizarse, ya que permite resolver posibles demoras [34]. En el caso de que el paciente requiera una consulta presencial, la realización de un cribado previo mediante cuestionarios relacionados con la sintomatología sugestiva de la COVID-19 (preferiblemente telemático), permitiría discriminar los distintos tipos de casos. Una vez acuda el paciente al centro hospitalario, se recomienda readaptar la sala de espera para que los pacientes puedan guardar una distancia de seguridad entre ellos de 2 metros y se deben eliminar de la consulta los objetos innecesarios, para facilitar el tránsito, orden, posterior limpieza y desinfección, así como tener previsión del material que vaya a ser usado [12,28]. Durante la consulta médica la puerta permanecerá cerrada, se asegurará la adecuada renovación del aire, y al finalizar, se mantendrá la habitación aireada al menos 15 minutos en niveles de alerta 2 o superior. Los filtros HEPA (High Efficiency Particulate Air) son capaces de filtrar en una sola pasada al menos el 99,97% de partículas de mayor o igual diámetro a 0,3 μm, y por ello deben ser tomados en cuenta en las tareas de desinfección del espacio de la consulta [36, 37].
El uso de povidona yodada (PVP-I) al 0,5% en gárgaras y gotas nasales podría utilizarse como como medida de precaución y seguridad durante la pandemia, ya que existe evidencia de que disminuye la concentración de virus SARS-CoV-1 [38,39], aunque no existe evidencia de que esta medida disminuya la transmisibilidad y puede inducir a una falsa sensación de seguridad [40].
Se recomiendan tomar medidas de precaución específicas durante los procedimientos no quirúrgicos en ORL en consulta y durante el ingreso hospitalario en planta (Tabla 3).
Tabla 3. Medidas de precaución específicas durante los procedimientos no quirúrgicos en ORL en consulta y durante el ingreso hospitalario en planta.
PROCEDIMIENTO |
RECOMENDACIÓN |
Endoscopia rígida o flexible |
- Uso de torre con cámara y pantalla para incrementar en lo posible la distancia entre el paciente y el explorador. - Evitar que el paciente se quite la mascarilla, sino que se la baje parcialmente. Como alternativa, se recomienda el uso de algún sistema que selle la nariz durante la exploración [12,41]. - Evitar manipulaciones endonasales innecesarias. - Reemplazar el uso del anestésico local en aerosol por mechas de algodón o lentinas empapadas en anestésico [42,43]. - En el caso de requerir taponamiento nasal por epistaxis aguda, o postquirúrgica, se recomienda el uso de taponamientos reabsorbibles [11,44]. - La retirada de un taponamiento nasal se realizará siguiendo las medidas de equipamiento en función de la clasificación del paciente (Tabla 2). - Desinfección con compuestos fenólicos, ácido peracético, o hipoclorito de sodio. Como alternativa se pueden utilizar fundas protectoras [45]. |
Otomicroscopio |
- Se recomienda utilizar material desechable. - Aunque estas exploraciones tienen un riesgo intermedio, se pueden adoptar medidas entre el microscopio y el paciente como pantallas de metacrilato adaptadas al binocular o envolventes de plástico desechables. - Tras la exploración con el microscopio, se limpiarán y se desinfectarán las zonas próximas o que hayan estado en contacto con el paciente, la lente y el área binocular del aparato [12,46]. |
Pruebas vestibulares |
- Se seguirán las recomendaciones de consulta general y las de audiometría (Tabla 4). |
Screening de audición para recién nacidos |
- Deberá ser realizado por personal que no trabaje directamente con pacientes COVID19, y si la madre está asintomática. - La protección del explorador se adaptará al grado de riesgo de contagio (Tabla 2), y a las medidas de protección general de la práctica ORL en consultas externas. - El equipo debe descontaminarse después de su uso. - Se recomienda que los niños nacidos durante la pandemia COVID-19 vuelvan a ser examinados cuando finalice la misma [47]. |
Cuidados postraqueotomía |
- En casos de pacientes con infección confirmada, se recomienda mantener el manguito inflado, usar un sistema de succión en línea y retrasar el cambio del tubo o cánula de traqueotomía hasta que se negativice la RT-PCR [48,49]. - En el resto de pacientes, se seguirán las recomendaciones de una maniobra con alto riesgo de generación de aerosoles. |
Dispositivos CPAP o BiPAP por síndrome de apnea obstructiva del sueño (AOS): |
- Al tratarse de dispositivos que generan aerosoles debido al sellado incompleto, se podría incrementar el riesgo de propagación del virus por vía aérea. - Se recomienda el uso de máscaras CPAP tipo casco para reducir el riesgo de transmisión [50,51]. |
Sospecha de aspiración de cuerpo extraño |
- Deben ser tomados en cuenta en tres situaciones fundamentalmente [47]: ○ La sospecha clínica de un cuerpo extraño es muy elevada (los padres han presenciado la aspiración de un cuerpo extraño, hay un claro síndrome de aspiración, tos persistente, disnea): la indicación debe mantenerse sin TC previo; ○ Se pone en duda la aspiración del cuerpo extraño (síndrome de aspiración sin anomalía clínica posterior o, por el contrario, compatible con la clínica (tos, asfixia, disnea, auscultación asimétrica), pero sin síndrome de aspiración franca o cualquier otra etiología obvia: se recomienda una TC de tórax que refuerce la sospecha previamente a la realización del abordaje endoscópico. ○ Caso con muy poca sospecha (sin síndrome de aspiración franco, sin anomalías clínicas sugestivas), no se recomienda ninguna TC ni endoscopia traqueobronquial. |
COVID-19(-): Caso descartado / COVID-19(¿): Caso probable o sospechoso / COVID-19(+): Caso confirmado [12].
Pruebas en cabinas de audiometría: se consideran espacios cerrados con un alto riesgo de acumulación de carga vírica, y de difícil desinfección, debiendo extremarse las precauciones durante estas exploraciones. Se recomienda que el paciente y el personal auxiliar entren con mascarilla a la cabina, lavado previo de las manos con solución hidroalcohólica, y guantes. El paciente debe sentarse en la silla sin tocar nada y las pruebas vocales se harán usando una grabación, nunca a viva voz (Tabla 4).
Tabla 4. Realización de la audiometría; indicación y medidas de protección del profesional y del paciente.
|
ESTADO DE CONTAGIOSIDAD Y GRAVEDAD DE LA HIPOACUSIA |
||
COVID-19 (-) |
COVID-19 (?) Y COVID-19 (+) |
||
INDICACIÓN TÉCNICA Y MATERIAL |
Sospecha de hipoacusia súbita |
Sin sospecha de hipoacusia súbita |
|
Audiometría de acto único o demora |
Realizar audiometría en el mismo acto (explicación previa escrita u oral facilitando la labiolectura del paciente) |
Demorar |
|
Utilización de cabina insonorizada |
Sí |
Según criterio clínico (se anotará en la HC si no se utiliza la cabina) |
|
Protección de cara, cabeza y manos del paciente |
Mascarilla quirúrgica |
FFP2, gorro desechable, lavado previo de manos y guantes |
|
Protección de auriculares |
Proteger con material desechable el auricular y el vibrador (preferiblemente usar auriculares de inserción de uso único) |
||
Indicación de respuesta positiva |
Levantando la mano, sin usar el pulsador |
||
Estimulación en audiometría vocal |
Usar grabación |
||
Limpieza tras finalizar la prueba |
1) audiómetro, 2) silla del paciente, 3) auricular, 4) vibrador, 5) limpiar y airear la cabina si se ha usado |
||
Cuando el paciente abandone la consulta, se retirará el material desechable en el contenedor destinado a ello, y se procederá a una minuciosa limpieza y desinfección de las superficies y zonas de contacto con el paciente, mediante una bayeta desechable o compresa no estéril, dejando actuar el producto durante unos minutos. Los productos de limpieza y desinfección habituales son eficaces frente a los coronavirus que pueden permanecer activos en superficies de plástico y de acero inoxidable entre 2-3 días [52], e incluso llegar hasta los 9 días en superficies no porosas [37]. Entre los más utilizados destacan la solución de hipoclorito sódico al 0,1%, y la solución hidroalcohólica aplicada preferiblemente con papel de un solo uso. En su defecto, se puede usar etanol (concentración de 62-71%) [45]. Manteniendo estos productos en las superficies durante un tiempo de exposición de 1 min se logran erradicar otros tipos de coronavirus, aunque no ha sido demostrado en el SARS-CoV-2 [37].
En relación al empleo de la luz ultravioleta (UV-C) para la desinfección, parece demostrada su eficacia para la esterilización de mascarillas [53] y también de las superficies sanitarias, aunque en este aspecto, hay consenso sobre que el mejor resultado se obtiene combinando la desinfección de las superficies y la aplicación de UV-C [54]. La Sociedad Española de Sanidad Ambiental (SESA) desaconseja el uso de dióxido de cloro para desinfectar el aire. El uso del ozono para la desinfección del aire y superficies requiere concentraciones elevadas con el consiguiente riesgo de toxicidad, por lo que se deben mantener los tiempos de descanso de las salas desinfectadas, restando eficiencia al método. Hasta la fecha, no hay certeza de que el incremento de las temperaturas con la llegada de la primavera, unido a la mayor radiación ultravioleta que alcanza la superficie de la tierra, puedan erradicar el coronavirus [55].
MEDIDAS ESPECÍFICAS Y TRANSVERSALES QUIRÚRGICAS
Las medidas de prevención llevadas a cabo por el equipo quirúrgico se realizan con el objetivo de proteger al propio equipo y al paciente. Se ha demostrado un alto riesgo de propagación del SARS-CoV-2 en la cirugía de la vía aerodigestiva en comparación a otras. Esto se explica por la alta carga viral detectada en la nasofaringe, asociada a la potencial aerosolización y diseminación de las partículas virales durante la instrumentación quirúrgica por el uso de fresas, microdebridadores, y/o bisturíes eléctricos o ultrasónicos, frecuentemente empleados en la cirugía ORL [11,50,56-58]. Se recomienda que en todo paciente que vaya a ser sometido a una cirugía de la vía aerodigestiva, se lleve a cabo el cribado en función del nivel de alerta en el que se encuentre la pandemia (Figura 1 y 2). Del mismo modo, es aconsejable firmar un consentimiento informado explícito [59], en el que se informe del riesgo que puede conllevar una intervención quirúrgica durante cualquiera de las fases de la pandemia.
Respecto a las medidas transversales del manejo en quirófano: Durante los periodos de alerta 4 se procurará postergar la cirugía electiva [60]. Debido a la elevada proporción de infectados asintomáticos, a priori debe asumirse todo paciente sin prueba que indique lo contrario como positivo para SARS-CoV-2 y tomar las medidas de protección como si lo fuera [60]. Si la situación lo permite se realizará un test de SARS-CoV-2 previo a la realización de una intervención quirúrgica tanto programada como urgente.
Se recomienda un entorno quirúrgico de presión negativa para reducir el riesgo de diseminación del SARS-CoV-2, mediante una alta frecuencia de cambios de aire (25 cambios por hora) que disminuya la carga viral en el interior del quirófano [61]. Se debería usar el mismo quirófano y el mismo equipo de anestesia para todos los pacientes COVID-19 probables o confirmados [61,62]. Esto incluye los casos emergentes en los que no se haya descartado la infección por SARS-CoV-2. Asimismo, durante las fases de nivel de alerta 2 o superior, se recomienda restringir el número de miembros del equipo quirúrgico [43]. En el momento de la inducción a la anestesia general, la intubación endotraqueal y los respiradores purificadores de aire serán obligatorios [63], debiendo encontrarse el paciente lo suficientemente profundizado durante la intervención para evitar despertares intraoperatorios. Se recomienda el uso de un sistema de aspiración cerrada con filtro antiviral [64].
Las partículas aerosolizadas de menos de 5 μm pueden permanecer en suspensión hasta más de 3 horas. Por este motivo, el uso de instrumental generador de aerosoles como los microdesbridadores o los motores de alta velocidad, así como instrumental generador de partículas en suspensión como los bisturíes eléctricos y los ultrasónicos deberá evitarse siempre que sea posible [52].
Las medidas de protección individuales se adaptarán según la clasificación del paciente (Tablas 5 y 6). En el postoperatorio inmediato, y a partir de que se establezca un nivel de alerta 2 o superior, la información a los familiares se realizará, preferiblemente, de forma telemática para reducir el movimiento del personal sanitario en el hospital [65]. El paciente intervenido pasará a la sala de reanimación, donde se tomarán las medidas propuestas por el servicio de anestesiología.
Tabla 5. Medidas protección del profesional en quirófano y durante procedimientos de riesgo fuera del quirófano.
MEDIDAS DE PROTECCIÓN INDIVIDUALES QUIRÚRGICAS |
|||
|
ESTADO INFECCIOSO DEL PACIENTE |
||
ZONA ANATÓMICA A PROTEGER |
COVID-19 (-) |
COVID-19 (¿) |
COVID-19 (+) NO DEMORABLE |
Pies |
Calzado laboral (zuecos) con calza desechable |
Calzado laboral (zuecos) con polaina desechable doble |
|
Cuerpo (Tronco y extremidades, excepto pies y manos) |
Pijama + bata quirúrgica desechables no impermeable |
Pijama + bata quirúrgica impermeable |
Pijama + EPI buzo + bata quirúrgica impermeable |
Cabeza (Cuero cabelludo, pabellón auricular y conducto auditivo externo) |
Gorro quirúrgico desechable |
Gorro quirúrgico estéril doble |
|
Manos |
Guante quirúrgico estéril simple |
Guante quirúrgico estéril doble |
|
Cara y cuello (Frente, cuello, región periauricular) |
Pantalla facial (opcional) |
Pantalla facial |
Escafandra o casco-pantalla integrados |
Ojos |
Gafa no integral |
Gafa integral |
Pantalla facial + gafa integral + proteger piel expuesta de frente, cuello y periauricular |
Respiratorio (Boca, orificios nasales y conducto auditivo externo) |
Mascarilla quirúrgica |
FFP3 |
FFP3 |
Tabla 6. Medidas protección del profesional en quirófano y durante procedimientos de riesgo fuera del quirófano.
MEDIDAS ESPECÍFICAS DURANTE LOS PROCEDIMIENTOS QUIRÚRGICOS O INVASIVOS EN ORL (Niveles de alerta 2 ó superior) |
|
Manejo de las vías respiratorias y procedimientos de diagnóstico de las vías respiratorias (excluyendo traqueostomía) [66] |
• Realización por el médico de mayor experiencia en técnicas de intubación de secuencia rápida. • Laringoscopios y videolaringoscopios desechables. • Evitar intubaciones con fibra óptica. • Realizar los procedimientos en vía aérea para pacientes con estado COVID-19 sospechoso, probable o positivo con intubación endotraqueal. • Minimizar la ventilación espontánea y la intubación / extubación repetida. |
Traqueotomía |
• La traqueotomía de emergencia confiere un riesgo significativo de aerosolización del virus y debe procederse con extrema precaución [63]. • Demorar la traqueotomía electiva, si es posible, hasta que el paciente infectado se negativice. • Los pacientes de traqueotomía COVID-19 (+) deben mantenerse en un circuito cerrado con succión en línea. • Retrasar los cambios de la cánula siempre que sea posible hasta que se resuelva la infección. Si es necesario realizarse en una sala de presión negativa con filtración HEPA y se debe utilizar un EPI mejorado, tipo buzo, para todo el personal [48,49]. |
Procedimientos de la cavidad oral, orofaringe, cavidad nasal y nasofaringe |
• Posponer los procedimientos que involucran la cavidad nasal, nasofaringe, cavidad oral y orofaringe en pacientes sospechosos, probables o positivos, siempre que sea posible, hasta la negativización (50). • Con el fin de evitar ingresos por sangrados postamigdalectomía, en el caso de tener que realizar este tipo de intervenciones, se recomienda el uso de la técnica con menor riesgo de complicaciones postoperatorias (amigdalectomía intracapsular) [47,67]. |
Cirugía otológica |
• Al no estar descartada la presencia del virus en las otitis medias con efusión [68], los procedimientos como los drenajes transtimpánicos deben evitarse [47,69]. • La mastoidectomía debe posponerse siempre que sea posible. Si se requiere mastoidectomía, se debe utilizar el EPI y se debe evitar el uso de motores de alta velocidad [70]. |
• Evitar el uso de microdesbridadores y/o los motores de alta resolución o fresas quirúrgicas siempre que sea posible. • En caso no poder demorar una intervención de base de cráneo anterior en un paciente COVID-19(+), se podría considerar un abordaje transcraneal, , a fin de evitar la cirugía nasosinusal, que presenta muchos más riesgo de aerosolización del virus [73]. El grado de afectación viral del tejido cerebral, aunque sospechado [74], parece mucho más bajo el nasosinusal, y, por tanto, su posible diseminación durante la intervención. • Usar taponamientos reabsorbibles en el postoperatorio. |
|
Cirugía de cabeza y cuello, y de los espacios profundos cervicales [75] |
• Se recomienda aplazar la exéresis quirúrgica de masas benignas del cuello durante las fases de alerta 2 ó superior. • Los pacientes pediátricos con tumores sólidos de cabeza y cuello, incluido el cáncer de tiroides, deben ser discutidos en una Comisión de tumores multidisciplinaria, para decidir la modalidad de tratamiento más adecuada, teniendo en cuenta la disponibilidad de recursos locales. • Los pacientes oncológicos de cabeza y cuello que requieran tratamiento quirúrgico, que hayan sido propuestos a tal efecto en la Comisión pertinente, tendrán prioridad sobre otros procedimientos no oncológicos, con independencia del nivel de alerta en el que se encuentre la pandemia. • Siempre que sea posible, se debe intentar el tratamiento médico de las enfermedades infecciosas antes de la intervención quirúrgica. |
COVID-19(-): Caso descartado / COVID-19(¿): Caso probable o sospechoso / COVID-19(+): Caso confirmado.
BIBLIOGRAFÍA
1. Zhou P, Yang X-L, Wang X-G, Hu B, Zhang L, Zhang W, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020 Mar;579(7798):270–3.
2. Lu R, Zhao X, Li J, Niu P, Yang B, Wu H, et al. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. The Lancet. 2020 Feb 22;395(10224):565–74.
3. Koh WC, Naing L, Chaw L, Rosledzana MA, Alikhan MF, Jamaludin SA, et al. What do we know about SARS-CoV-2 transmission? A systematic review and meta-analysis of the secondary attack rate and associated risk factors. PloS One. 2020;15(10):e0240205.
4. Bax A, Bax CE, Stadnytskyi V, Anfinrud P. SARS-CoV-2 transmission via speech-generated respiratory droplets. Lancet Infect Dis. 2020 Sep 11
5. Wassie GT, Azene AG, Bantie GM, Dessie G, Aragaw AM. Incubation Period of Severe Acute Respiratory Syndrome Novel Coronavirus 2 that Causes Coronavirus Disease 2019: A Systematic Review and Meta-Analysis. Curr Ther Res Clin Exp. 2020;93:100607.
6. He J, Guo Y, Mao R, Zhang J. Proportion of asymptomatic coronavirus disease 2019: A systematic review and meta-analysis. J Med Virol. 2021 Feb;93(2):820–30.
7. Meyerowitz-Katz G, Merone L. A systematic review and meta-analysis of published research data on COVID-19 infection fatality rates. Int J Infect Dis IJID Off Publ Int Soc Infect Dis. 2020 Dec;101:138–48.
8. Levin AT, Hanage WP, Owusu-Boaitey N, Cochran KB, Walsh SP, Meyerowitz-Katz G. Assessing the age specificity of infection fatality rates for COVID-19: systematic review, meta-analysis, and public policy implications. Eur J Epidemiol. 2020 Dec;35(12):1123–38.
9. Sayampanathan AA, Heng CS, Pin PH, Pang J, Leong TY, Lee VJ. Infectivity of asymptomatic versus symptomatic COVID-19. Lancet Lond Engl. 2021 Jan 9;397(10269):93–4.
10. Sahu AK, Amrithanand VT, Mathew R, Aggarwal P, Nayer J, Bhoi S. COVID-19 in health care workers - A systematic review and meta-analysis. Am J Emerg Med. 2020 Sep;38(9):1727–31.
11. Workman AD, Welling DB, Carter BS, Curry WT, Holbrook EH, Gray ST, et al. Endonasal instrumentation and aerosolization risk in the era of COVID-19: simulation, literature review, and proposed mitigation strategies. Int Forum Allergy Rhinol. 2020 Apr 3
12. Maza-Solano JM, Plaza-Mayor G, Jiménez-Luna A, Parente-Arias P, Amor-Dorado JC. Strategies for the Practice of Otolaryngology and Head and Neck Surgery During the Monitoring Phase of COVID-19. Acta Otorrinolaringol Esp. 2020;71(6):367–78.
13. Martin-Villares C, Bernal-Sprekelsen M, Molina-Ramirez CP, Bartolome-Benito M. Risk of contagion of SARS-CoV-2 among otorhinolaryngologists in Spain during the “Two waves”. Eur Arch Oto-Rhino-Laryngol Off J Eur Fed Oto-Rhino-Laryngol Soc EUFOS Affil Ger Soc Oto-Rhino-Laryngol - Head Neck Surg. 2021 Jan 19;1–7.
14. Actuaciones de respuesta coordinada para el control de la transmisión de COVID-19 In: Sanidad Md, editor. 2020 [Internet]. [Internet]. [citado 2021 Ene 31]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/Actuaciones_respuesta_COVID_22.10.2020.pdf
15. Estrategia de detección precoz, vigilancia y control de COVID-19. In: Sanidad Md, editor. 2020. [Internet] [Internet]. 2020 [citado 2021 Feb 15]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/COVID19_Estrategia_vigilancia_y_control_e_indicadores.pdf
16. Wölfel R, Corman VM, Guggemos W, Seilmaier M, Zange S, Müller MA, et al. Virological assessment of hospitalized patients with COVID-2019. Nature [Internet]. 2020 Abr 1; Disponible en: https://doi.org/10.1038/s41586-020-2196-x
17. Altmann DM, Douek DC, Boyton RJ. What policy makers need to know about COVID-19 protective immunity. The Lancet [Internet]. [citado 2020 Abr 29]; Disponible en: https://doi.org/10.1016/S0140-6736(20)30985-5
18. Wu F, Wang A, Liu M, Wang Q, Chen J, Xia S, et al. Neutralizing antibody responses to SARS-CoV-2 in a COVID-19 recovered patient cohort and their implications. medRxiv. 2020 Jan 1;2020.03.30.20047365.
19. Tan W, Lu Y, Zhang J, Wang J, Dan Y, Tan Z, et al. Viral Kinetics and Antibody Responses in Patients with COVID-19. medRxiv. 2020 Jan 1;2020.03.24.20042382.
20. Zhao J, Yuan Q, Wang H, Liu W, Liao X, Su Y, et al. Antibody responses to SARS-CoV-2 in patients of novel coronavirus disease 2019. Clin Infect Dis Off Publ Infect Dis Soc Am. 2020 Mar 28
21. Grupo de expertos SEIMC para el análisis del diagnóstico microbiológico del COVID-19. Recomendaciones institucionales. Documento de posicionamiento de la SEIMC sobre el diagnóstico microbiológico de COVID-19 [Internet]. [citado 2021 Feb 15]. Disponible en: https://seimc.org/contenidos/documentoscientificos/recomendaciones/seimc-rc-2020-Posicionamiento_SEIMC_diagnostico_microbiologico_COVID19.pdf
22. Petherick A. Developing antibody tests for SARS-CoV-2. Lancet Lond Engl. 2020 Apr 4;395(10230):1101–2.
23. Cevik M, Tate M, Lloyd O, Maraolo AE, Schafers J, Ho A. SARS-CoV-2, SARS-CoV, and MERS-CoV viral load dynamics, duration of viral shedding, and infectiousness: a systematic review and meta-analysis. Lancet Microbe. 2021 Jan 1;2(1):e13–22.
24. European Centre for Disease Prevention and Control. Guidance for discharge and ending isolation of people with COVID-19, 16 October 2020. Stockholm: ECDC; 2020.
25. Actuaciones de respuesta coordinada para el control de la transmisión de COVID-19 In: Sanidad Md, editor. 2020.
26. Recomendaciones para la programación de cirugía en condiciones de seguridad durante la pandemia COVID-19. Versión 14 de diciembre 2020. Coordinación: Área de Calidad de la Subdirección General de Promoción, Prevención y Calidad Centro de Coordinación de Alertas y Emergencias Sanitarias Dirección General de Salud Pública. Ministerio de Sanidad. [Internet]. [citado 2021 Ene 31]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/COVID19_Cirugia_electiva.pdf
27. Zou L, Ruan F, Huang M, Liang L, Huang H, Hong Z, et al. SARS-CoV-2 Viral Load in Upper Respiratory Specimens of Infected Patients. N Engl J Med. 2020 Feb 19;382(12):1177–9.
28. Brücher BLDM, Nigri G, Tinelli A, Lapeña JFF, Espin-Basany E, Macri P, et al. COVID-19: Pandemic surgery guidance. 4open [Internet]. 2020;3. Disponible en: https://doi.org/10.1051/fopen/2020002
29. Bartoszko JJ, Farooqi MAM, Alhazzani W, Loeb M. Medical masks vs N95 respirators for preventing COVID-19 in healthcare workers: A systematic review and meta-analysis of randomized trials. Influenza Other Respir Viruses. 2020 Apr 4
30. WHO. Sus 5 momentos para la higiene de manos. [Internet]. [citado 2021 Jan 31]. Disponible en: https://www.who.int/gpsc/information_centre/gpsc_5_momentos_poster_es.pdf?ua=1
31. WHO. La higiene de manos y el recorrido del paciente quirúrgico. [Internet]. [citado 2021 Ene 31]. Disponible en: https://www.who.int/gpsc/5may/hh_infographic_A3_ES.pdf?ua=1
32. Liu Z, Zhang L. At the center of the COVID-19 pandemic: Lessons learned for otolaryngology-head and neck surgery in China. Int Forum Allergy Rhinol. 2020 May;10(5):584–6.
33. Documento técnico. Manejo en atención primaria y domiciliaria del COVID-19 [Internet]. 2020 [citado 2021 Ene 28]. Disponible en: https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov-China/documentos/Manejo_primaria.pdf
34. Asadi S, Wexler AS, Cappa CD, Barreda S, Bouvier NM, Ristenpart WD. Aerosol emission and superemission during human speech increase with voice loudness. Sci Rep. 2019 Feb 20;9(1):2348.
35. Ning AY, Cabrera CI, D’Anza B. Telemedicine in Otolaryngology: A Systematic Review of Image Quality, Diagnostic Concordance, and Patient and Provider Satisfaction. Ann Otol Rhinol Laryngol. 2021 Feb;130(2):195–204.
36. Kampf G, Todt D, Pfaender S, Steinmann E. Persistence of coronaviruses on inanimate surfaces and their inactivation with biocidal agents. J Hosp Infect. 2020 Mar 1;104(3):246–51.
37. Khan MM, Parab SR. 0.5% povidone iodine irrigation in otorhinolaryngology surgical practice during COVID 19 pandemic. Am J Otolaryngol. 2020 Dec;41(6):102687.
38. Frank S, Capriotti J, Brown SM, Tessema B. Povidone-Iodine Use in Sinonasal and Oral Cavities: A Review of Safety in the. Ear Nose Throat J. 2020 Nov;99(9):586–93.
39. Burton MJ, Clarkson JE, Goulao B, Glenny A-M, McBain AJ, Schilder AGM, Webster KE, Worthington HV. Antimicrobial mouthwashes (gargling) and nasal sprays administered to patients with suspected or confirmed COVID-19 infection to improve patient outcomes and to protect healthcare workers treating them. Cochrane Database of Systematic Reviews 2020, Issue 9. Art. No.: CD013627. DOI: 10.1002/14651858.CD013627.pub2.
40. Lechien JR, Chiesa-Estomba CM, De Siati DR, Horoi M, Le Bon SD, Rodriguez A, et al. Olfactory and gustatory dysfunctions as a clinical presentation of mild-to-moderate forms of the coronavirus disease (COVID-19): a multicenter European study. Eur Arch Otorhinolaryngol [Internet]. 2020 Abr 6; Disponible en: https://doi.org/10.1007/s00405-020-05965-1
41. Kamming D, Gardam M, Chung F. Anaesthesia and SARS. Br J Anaesth. 2003 Jun;90(6):715–8.
42. Van Gerven L, Hellings PW, Cox T, Fokkens W, Hopkins C, Hox V, et al. Personal protection and delivery of rhinologic and endoscopic skull base procedures during the COVID-19 outbreak. Rhinol J. 2020 Apr 1
43. Workman AD, Jafari A, Welling DB, Varvares MA, Gray ST, Holbrook EH, et al. Airborne Aerosol Generation During Endonasal Procedures in the Era of COVID-19: Risks and Recommendations. Otolaryngol Neck Surg. 2020 May 26;163(3):465–70.
44. List N: Disinfectants for Use Against SARS-CoV-2 [Internet]. 2020 [citado 2021 Jul 2]. Disponible en: List N: Disinfectants for Use Against SARS-CoV-2. United States Environmental Protection Agency. https://www.epa.gov/pesticide-registration/list-n-disinfectants-useagainst-sars-cov-2. Published 2020).
45. Lavilla MJ, Huarte A, Cavallé L, Núñez F. Medidas de desinfección e higiene en audiología y estrategias comunicativas durante pandemia COVID-19 [Internet]. [citado 2021 Feb 16]. Disponible en: https://seorl.net/wp-content/uploads/2020/04/MEDIDAS-DE-DESINFECCIÓN-E-HIGIENE-EN-AUDIOLOGÍA-Y-ESTRATEGIAS-COMUNICATIVAS-DURANTE-LA-PANDEMIA-COVID-19.pdf
46. Leboulanger N, Sagardoy T, Akkari M, Ayari-Khalfallah S, Celerier C, Fayoux P, et al. COVID-19 and ENT Pediatric otolaryngology during the COVID-19 pandemic. Guidelines of the French Association of Pediatric Otorhinolaryngology (AFOP) and French Society of Otorhinolaryngology (SFORL). Eur Ann Otorhinolaryngol Head Neck Dis. 2020 May;137(3):177–81.
47. Díaz de Cerio Canduela P, Ferrandis Perepérez E, Parente Arias P, López Álvarez F, Sistiaga Suarez JA. Recommendations of the Spanish Society of Otolaryngology and Head and Neck Surgery for performing tracheotomies in patients infected by the coronavirus, Covid-19. Acta Otorrinolaringol Esp. 2020 Aug;71(4):253–5.
48. Martin-Villares C, Perez Molina-Ramirez C, Bartolome-Benito M, Bernal-Sprekelsen M. Outcome of 1890 tracheostomies for critical COVID-19 patients: a national cohort study in Spain. Eur Arch Oto-Rhino-Laryngol Off J Eur Fed Oto-Rhino-Laryngol Soc EUFOS Affil Ger Soc Oto-Rhino-Laryngol - Head Neck Surg. 2020 Aug 4;1–8.
49. Bann DV, Patel VA, Saadi R, Gniady JP, Goyal N, McGinn JD, et al. Impact of Coronavirus (COVID-19) on Otolaryngologic Surgery: A Brief Commentary. Head Neck. 2020 Apr 9
50. Tran K, Cimon K, Severn M, Pessoa-Silva CL, Conly J. Aerosol generating procedures and risk of transmission of acute respiratory infections to healthcare workers: a systematic review. PloS One. 2012;7(4):e35797.
51. van Doremalen N, Bushmaker T, Morris DH, Holbrook MG, Gamble A, Williamson BN, et al. Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV-1. N Engl J Med. 2020 Mar 17
52. Hamzavi IH, Lyons AB, Kohli I, Narla S, Parks-Miller A, Gelfand JM, et al. Ultraviolet germicidal irradiation: possible method for respirator disinfection to facilitate reuse during COVID-19 pandemic. J Am Acad Dermatol. 2020 Apr 1
53. Dexter F, Parra MC, Brown JR, Loftus RW. Perioperative COVID-19 Defense: An Evidence-Based Approach for Optimization of Infection Control and Operating Room Management. Anesth Analg. 2020 Mar 26
54. Patel R, Babady E, Theel ES, Storch GA, Pinsky BA, St George K, et al. Report from the American Society for Microbiology COVID-19 International Summit, 23 March 2020: Value of Diagnostic Testing for SARS-CoV-2/COVID-19. mBio. 2020 Mar 26;11(2).
55. Lauer SA, Grantz KH, Bi Q, Jones FK, Zheng Q, Meredith HR, et al. The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application. Ann Intern Med. 2020 Mar 10
56. Wang J, Zhou M, Liu F. Reasons for healthcare workers becoming infected with novel coronavirus disease 2019 (COVID-19) in China. J Hosp Infect. 2020 Mar 6
57. Sociedad Española de Otorrinolaringología y Cirugía de Cabeza y Cuello (SEORLCCC). Documento de información y autorización para la realización de exploraciones e intervenciones quirúrgicas durante la pandemia por COVID-19 [Internet]. [citado 2021 Feb 15]. Disponible en: https://seorl.net/wp-content/uploads/2020/05/documento-de-informacion-y-autorizacion-para-la-realizacion-de-exploraciones-e-intervenciones-qx-durante-la-pandemia-por-covid-19.pdf
58. Somashekhar SP, Shivaram HV, Abhaham SJ, Dalvi A, Kumar A, Gode D, et al. ASI’s Consensus Guidelines: ABCs of What to Do and What Not During the COVID-19 Pandemic. Indian J Surg. 2020 Jun 1;82(3):240–50.
59. Kowalski LP, Sanabria A, Ridge JA, Ng WT, de Bree R, Rinaldo A, et al. COVID-19 pandemic: effects and evidence-based recommendations for otolaryngology and head and neck surgery practice. Head Neck. 2020 Apr 9
60. Ti LK, Ang LS, Foong TW, Ng BSW. What we do when a COVID-19 patient needs an operation: operating room preparation and guidance. Can J Anaesth J Can Anesth. 2020 Mar 6
61. Wax RS, Christian MD. Practical recommendations for critical care and anesthesiology teams caring for novel coronavirus (2019-nCoV) patients. Can J Anaesth J Can Anesth. 2020 Feb 12
62. Martín Delgado MC, Avilés-Jurado FX, Álvarez Escudero J, Aldecoa Álvarez-Santuyano C, de Haro López C, Díaz de Cerio Canduela P, et al. Consensus document of the Spanish Society of Intensive and Critical Care Medicine and Coronary Units (SEMICYUC), the Spanish Society of Otorhinolaryngology and Head and Neck Surgery (SEORL-CCC) and the Spanish Society of Anesthesiology and Resuscitation (SEDAR) on tracheotomy in patients with COVID-19 infection. Med Intensiva Engl Ed. 2020;44(8):493–9.
63. Prin M, Bartels K. Social distancing: implications for the operating room in the face of COVID-19. Can J Anaesth J Can Anesth. 2020 Apr 14
64. Villalonga Vadell R, Martín Delgado MC, Avilés-Jurado FX, Álvarez Escudero J, Aldecoa Álvarez-Santuyano C, de Haro López C, et al. Consensus Document of the Spanish Society of Intensive and Critical Care Medicine and Coronary Units (SEMICYUC), the Spanish Society of Otorhinolaryngology and Head and Neck Surgery (SEORL-CCC) and the Spanish Society of Anesthesiology and Resuscitation (SEDAR) on Tracheotomy in Patients with COVID-19 Infection. Rev Esp Anestesiol Reanim. 2020 Nov;67(9):504–10.
65. Comisión de Otorrinolaringología Pediátrica, Grupo de trabajo en COVID, Comisión delegada de la SEORLCCC. Recomendaciones en el manejo del paciente pediátrico en el contexto de la pandemia por COVID-19 [Internet]. [Internet]. [citado 2021 Jan 31]. Disponible en: https://seorl.net/wp-content/uploads/2020/03/RECOMENDACIONES-EN-EL-MANEJO-DEL-PACIENTE-PEDIÁTRICO-EN-EL-CONTEXTO-DE-LA-PANDEMIA-POR-COVID-19-1.pdf
66. Maharaj S, Bello Alvarez M, Mungul S, Hari K. Otologic dysfunction in patients with COVID-19: A systematic review. Laryngoscope Investig Otolaryngol. 2020 Dec;5(6):1192–6.
67. Chorney SR, Elden LM, Giordano T, Kazahaya K, Rizzi MD, Zur KB, et al. Algorithm-Based Pediatric Otolaryngology Management During the COVID-19 Global Pandemic: A Children’s Hospital of Philadelphia Clinical Consensus. Otolaryngol--Head Neck Surg Off J Am Acad Otolaryngol-Head Neck Surg. 2020 Jul;163(1):25–37.
68. Markey AL, Leong SC, Vaughan C. Droplet and bone dust contamination from high-speed drilling during mastoidectomy. Clin Otolaryngol Off J ENT-UK Off J Neth Soc Oto-Rhino-Laryngol Cervico-Facial Surg. 2021 Feb 3
69. Jones HAS, Salib RJ, Harries PG. Reducing Aerosolized Particles and Droplet Spread in Endoscopic Sinus Surgery during. The Laryngoscope. 2020 Aug 15
70. Viera-Artiles J, Mato D, Valdiande JJ, Lobo D, Pedraja J, López-Higuera JM, et al. A novel aerosolisation mitigation device for endoscopic sinus and skull base surgery in the COVID-19 era. Eur Arch Oto-Rhino-Laryngol Off J Eur Fed Oto-Rhino-Laryngol Soc EUFOS Affil Ger Soc Oto-Rhino-Laryngol - Head Neck Surg. 2020 Nov 16;1–9.
71. Patel ZM, Fernandez-Miranda J, Hwang PH, Nayak JV, Dodd R, Sajjadi H, et al. Precautions for endoscopic transnasal skull base surgery during the COVID-19 pandemic. Neurosurg 2020E-Pub Ahead Prin [Internet]. Disponible en: https://operativeneurosurgery.com/doku.php?id=precautions_for_endoscopic_transnasal_skull_base_surgery_during_the_covid-19_pandemic
72. Kabbani N, Olds JL. Does COVID19 Infect the Brain? If So, Smokers Might Be at a Higher Risk. Mol Pharmacol. 2020 May;97(5):351–3.
73. Bann DV, Patel VA, Saadi R, Goyal N, Gniady JP, McGinn JD, et al. Best Practice Recommendations for Pediatric Otolaryngology during the COVID-19 Pandemic. Otolaryngol--Head Neck Surg Off J Am Acad Otolaryngol-Head Neck Surg. 2020 Jun;162(6):783–94.